千葉大研究チーム、がんを支える遺伝子発現を調節する因子を新たに発見
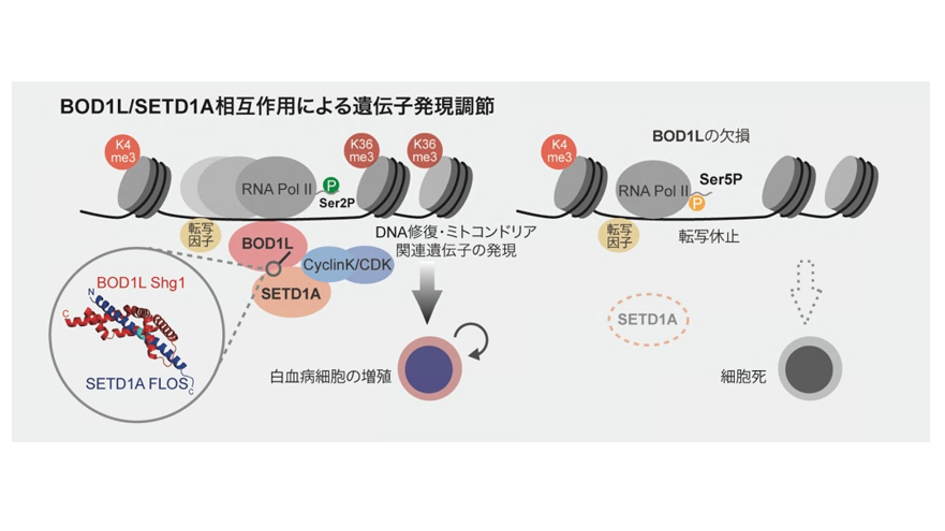
千葉大学大学院医学研究院の星居孝之准教授、金田篤志教授らの研究チームは、急性骨髄性白血病細胞の中で働く遺伝子発現の新しい調節因子BOD1Lを発見した。BOD1Lはヒストンメチル化酵素であるSETD1Aを直接的に制御する因子として作用しており、この2つの遺伝子の相互作用を破壊すると白血病細胞が死滅することが確認された。
さらに詳しい解析により、BOD1LはSETD1Aの古典的な役割であるヒストンメチル化機能とは異なる遺伝子発現調節機構を司ることによって、白血病細胞の生存に必須となることが明らかとなった。このことからBOD1Lは、がんの新たな治療標的になると考えられる。
研究チームはDepMapデータベースを基にSETD1Aと共依存性を示す分子を探索し、DNA修復制御因子BOD1Lを同定した。CRISPRタイリング法を活用した機能解析により、BOD1Lが白血病細胞の生存に必須となることを発見した。
また、BOD1LとSETD1Aをそれぞれ欠損する白血病細胞で発現低下する遺伝子群はほぼ同一であり、BOD1L欠損時に観察される核内変化もSETD1Aを欠損した際の結果と同じであった。BOD1L欠損時には核内のDNA上からSETD1Aタンパク質が速やかに消失することから、BOD1LはSETD1AのDNA結合の主導的な制御因子であることが分かった。
AIシステムを使ったタンパク質複合体の予測から、BOD1LとSETD1Aが結びつく様子が予測され、BOD1Lタンパク質はSETD1Aタンパク質の一部に巻きつく特徴的な形をしており、新たな創薬標的として有用であることが示唆された。
split-TurboIDを活用した解析の結果から、多数の転写制御因子がこの複合体と連携して作用していることも分かった。以上の結果から、BOD1LはSETD1Aと結合することにより、DNA修復制御因子としてよりも、がんの増殖や生存を助ける転写促進因子として働くことが明らかとなった。
本研究成果は、科学誌Nucleic Acids Researchにて2024年7月12日にオンライン公開された。